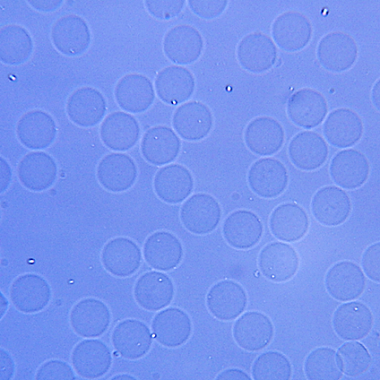
単分散で再現性のあるハイドロゲルビーズ
マイクロ流体チップを用いることで、直径数µm〜数百µmの単分散マイクロハイドロゲルビーズをハイスループットかつ高再現性で作製できます。アガロース、ヒアルロン酸、アルギン酸などの多糖類、ゼラチンやコラーゲンなどのタンパク質、PEGDAなどの樹脂材料まで、幅広い組成に対応可能です。
主なハイドロゲルの種類
| 材質 | ゲル化方法 | 生成装置 |
|---|---|---|
| コラーゲン | 温度差 | MDGMD |
| アガロース | 温度差 | MDGMD |
| ゼラチン | 架橋結合 | MDGMD |
| アルギン酸 | カルシウム塩添加析出 | MDGMD |
| ポリエチレングリコールジアクリレート (PEGDA) | 光硬化 | MDGMD |
近年は新規生体適合性ハイドロゲルの開発が進んでおり、研究・応用範囲はさらに拡大しています。
マイクロハイドロゲルビーズの用途例
- 3D細胞培養・スフェロイド作製
- 抗体アッセイ
- ハイスループットスクリーニング
- ドラッグデリバリーシステム(DDS)研究
- 生体・抗体医薬DDS研究
- シングルセル解析・イメージング
- 化粧品材料
- 食品・サプリメント材料
- 新材料・素材研究開発
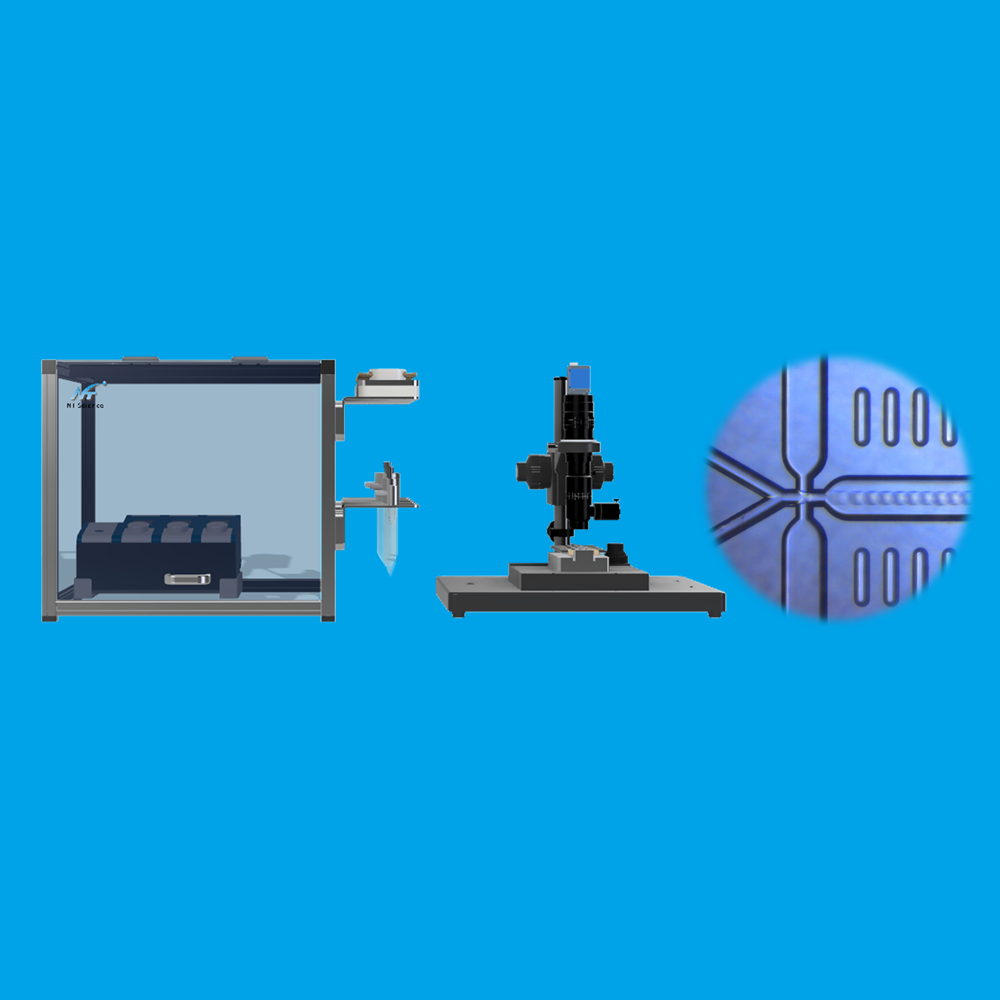
マイクロ流体チップを用いたマイクロハイドロゲル作製
両側から交差する油相流により、定量かつ均一な水相ドロップレットが連続的に形成されます。ドロップレット形成直前に2液を混合する設計は、細胞封入型三次元培養やバイオアッセイ開発に適しています。
マイクロドロップレットジェネレーター MDGMD
マイクロドロップレットジェネレーター MDGMDは、単分散ドロップレットおよびハイドロゲル生成に特化した研究用ドロップレットジェネレーターです。学術研究および研究開発用途において、高い再現性と操作性を提供します。
参考文献
- Akselband, Y et al. “Rapid mycobacteria drug susceptibility testing using Gel Microdrop (GMD) Growth Assay and flow cytometry.” Journal of microbiological methods vol. 62,2 (2005): 181-97. doi:10.1016/j.mimet.2005.02.012
- Benavente-Babace, Ainara et al. “Strategies for controlling egress of therapeutic cells from hydrogel microcapsules.” Journal of tissue engineering and regenerative medicine vol. 13,4 (2019): 612-624. doi:10.1002/term.2818
- Brinkmann, Stephan et al. “Two-step generation of monodisperse agarose-solidified double emulsions (w/w/o) excluding an inner oil barrier.” MethodsX vol. 8 101565. 2 Nov. 2021, doi:10.1016/j.mex.2021.101565
- Chokkalingam V, Tel J, Wimmers F, et al. Probing cellular heterogeneity in cytokine-secreting immune cells using droplet-based microfluidics. Lab Chip. 2013;13(24):4740-4744. doi:10.1039/c3lc50945a
- Chung, Casper H Y et al. “Droplet-Based Microfluidic Synthesis of Hydrogel Microparticles via Click Chemistry-Based Cross-Linking for the Controlled Release of Proteins.” ACS applied bio materials vol. 4,8 (2021): 6186-6194. doi:10.1021/acsabm.1c00509
- De Rop, Florian V et al. “Hydrop enables droplet-based single-cell ATAC-seq and single-cell RNA-seq using dissolvable hydrogel beads.” eLife vol. 11 e73971. 23 Feb. 2022, doi:10.7554/eLife.73971
- Eun, Ye-Jin et al. “Encapsulating bacteria in agarose microparticles using microfluidics for high-throughput cell analysis and isolation.” ACS chemical biology vol. 6,3 (2011): 260-6. doi:10.1021/cb100336p
- Geng, Tao, and Richard A Mathies. “Minimizing inhibition of PCR-STR typing using digital agarose droplet microfluidics.” Forensic science international. Genetics vol. 14 (2015): 203-9. doi:10.1016/j.fsigen.2014.10.007
- Hauck N, Seixas N, Centeno SP, et al. Droplet-Assisted Microfluidic Fabrication and Characterization of Multifunctional Polysaccharide Microgels Formed by Multicomponent Reactions. Polymers (Basel). 2018;10(10):1055. Published 2018 Sep 21. doi:10.3390/polym10101055
- Hosokawa, Masahito et al. “Droplet-based microfluidics for high-throughput screening of a metagenomic library for isolation of microbial enzymes.” Biosensors & bioelectronics vol. 67 (2015): 379-85. doi:10.1016/j.bios.2014.08.059
- Jang, Minjeong et al. “Droplet-based microtumor model to assess cell-ECM interactions and drug resistance of gastric cancer cells.” Scientific reports vol. 7 41541. 27 Jan. 2017, doi:10.1038/srep41541
- Kumachev, Alexander et al. “High-throughput generation of hydrogel microbeads with varying elasticity for cell encapsulation.” Biomaterials vol. 32,6 (2011): 1477-83. doi:10.1016/j.biomaterials.2010.10.033
- Laperrousaz, B et al. “Direct transfection of clonal organoids in Matrigel microbeads: a promising approach toward organoid-based genetic screens.” Nucleic Acids Res. 2018 Jul 6;46(12):e70. doi: 10.1093/nar/gky030.
- Leng, Xuefei et al. “Agarose droplet microfluidics for highly parallel and efficient single molecule emulsion PCR.” Lab on a chip vol. 10,21 (2010): 2841-3. doi:10.1039/c0lc00145g
- Li M, Liu H, Zhuang S, Goda K. Droplet flow cytometry for single-cell analysis. RSC Adv. 2021;11(34):20944-20960. Published 2021 Jun 14. doi:10.1039/d1ra02636d
- Ma C, Tan ZL, Lin Y, Han S, Xing X, Zhang C. Gel microdroplet-based high-throughput screening for directed evolution of xylanase-producing Pichia pastoris. J Biosci Bioeng. 2019;128(6):662-668. doi:10.1016/j.jbiosc.2019.05.008
- Mahler, Lisa et al. “Highly parallelized droplet cultivation and prioritization of antibiotic producers from natural microbial communities.” eLife vol. 10 e64774. 25 Mar. 2021, doi:10.7554/eLife.64774
- Oberpaul, Markus et al. “Combination of high-throughput microfluidics and FACS technologies to leverage the numbers game in natural product discovery.” Microbial biotechnology vol. 15,2 (2022): 415-430. doi:10.1111/1751-7915.13872
- Okubanjo, Sewuese S et al. “The use of confocal Raman microscopy and microfluidic channels to monitor the location and mobility of β-carotene incorporated in droplet-stabilized oil-in-water emulsions.” Current research in food science vol. 6 100515. 13 May. 2023, doi:10.1016/j.crfs.2023.100515
- Ou, Yangteng et al. “Droplet microfluidics on analysis of pathogenic microbes for wastewater-based epidemiology.” Trends in analytical chemistry : TRAC vol. 143 (2021): 116333. doi:10.1016/j.trac.2021.116333
- Schaerli, Yolanda. “Bacterial Microcolonies in Gel Beads for High-throughput Screening.” Bio-protocol vol. 8,13 (2018): e2911. doi:10.21769/BioProtoc.2911
- Sinha N, Subedi N, Tel J. Integrating Immunology and Microfluidics for Single Immune Cell Analysis. Front Immunol. 2018;9:2373. Published 2018 Oct 16. doi:10.3389/fimmu.2018.02373
- Shijo, Seito et al. “Dielectrophoresis-Based Selective Droplet Extraction Microfluidic Device for Single-Cell Analysis.” Micromachines vol. 14,3 706. 22 Mar. 2023, doi:10.3390/mi14030706
- Tiemeijer BM, Tel J. Hydrogels for Single-Cell Microgel Production: Recent Advances and Applications. Front Bioeng Biotechnol. 2022;10:891461. Published 2022 Jun 17. doi:10.3389/fbioe.2022.891461
- Tiemeijer, Bart M et al. “A Microfluidic Approach for Probing Heterogeneity in Cytotoxic T-Cells by Cell Pairing in Hydrogel Droplets.” Micromachines vol. 13,11 1910. 4 Nov. 2022, doi:10.3390/mi13111910
- van Tatenhove-Pel RJ, Hernandez-Valdes JA, Teusink B, Kuipers OP, Fischlechner M, Bachmann H. Microdroplet screening and selection for improved microbial production of extracellular compounds. Curr Opin Biotechnol. 2020;61:72-81. doi:10.1016/j.copbio.2019.10.007
- Yanakieva, Desislava et al. “FACS-Based Functional Protein Screening via Microfluidic Co-encapsulation of Yeast Secretor and Mammalian Reporter Cells.” Scientific reports vol. 10,1 10182. 23 Jun. 2020, doi:10.1038/s41598-020-66927-5
- Zamora-Mora, Vanessa et al. “Chitosan/agarose hydrogels: cooperative properties and microfluidic preparation.” Carbohydrate polymers vol. 111 (2014): 348-55. doi:10.1016/j.carbpol.2014.04.087
- Zhang, Lexiang et al. “Near-Infrared Responsive Droplet for Digital PCR.” Small (Weinheim an der Bergstrasse, Germany) vol. 18,16 (2022): e2107858. doi:10.1002/smll.202107858
- Zhu, Zhi et al. “Highly sensitive and quantitative detection of rare pathogens through agarose droplet microfluidic emulsion PCR at the single-cell level.” Lab on a chip vol. 12,20 (2012): 3907-13. doi:10.1039/c2lc40461c

NTサイエンスへのお問い合わせ内容には、通常2営業日以内にご返信致します。
※装置や特注品の御見積は、通常よりもお時間を要する場合がありますので、予めご了承ください。
旧来の050IP電話番号廃止のお知らせ:
事業者のサービス終了に伴い、050-5539で始まる番号は2025年3月31日をもって廃止となりました。
製品お問い合わせや見積依頼は下記お問い合わせフォーム、メール又はFAXにてお願い致します。
ご回答以外の不要な営業アプローチをすることはありませんのでお気軽にお問い合わせください。
◆お問い合わせフォーム
※営業・セールス、スパム、迷惑行為は禁止です。
その他連絡先
◆メール
![]()
※営業・セールス、スパム、迷惑行為は禁止です。
※nt-science.com からのメールをブロック解除し、迷惑メールフォルダをご確認ください。
◆FAX
![]()
※当日受注分:平日17:30まで(土日祝日、休業期間を除く)