mRNA封入脂質ナノ粒子(mRNA-LNP)生成に最適
脂質ナノ粒子(LNP)/リポソーム生成チップキット LNPSCは、mRNA封入脂質ナノ粒子(mRNA-LNP)をはじめとする各種ナノ粒子を生成するためのガラス製マイクロ流路チップです。
マイクロ流体技術は、従来のバルク混合法と比較して、ナノ粒子の粒子径の均一性や内包物の封入効率を高め、再現性の高い生成を実現します。少量試料での検討が可能なため、安全かつ効率的に条件探索を進められ、LNPなどのナノ粒子の研究開発に適しています。
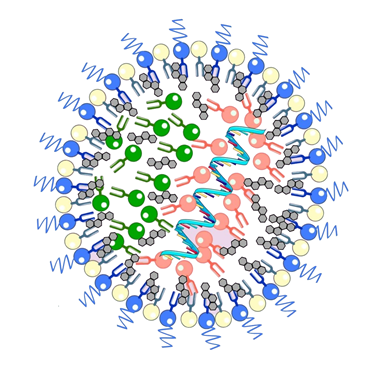
mRNA封入脂質ナノ粒子(mRNA-LNP)は、遺伝子情報を細胞内へ効率的に送達するための技術で、mRNAワクチン開発において重要な役割を担ってきました。RNAなど生体分解性が高い分子をLNPへ内包して送達するDDS(Drug Delivery System)は、ワクチンに限らず、がんや遺伝性疾患などへの応用が期待されています。
主な用途(研究領域)
チップ構造(混合方式)
Hydrodynamic Flow Focusing(HFF)タイプ
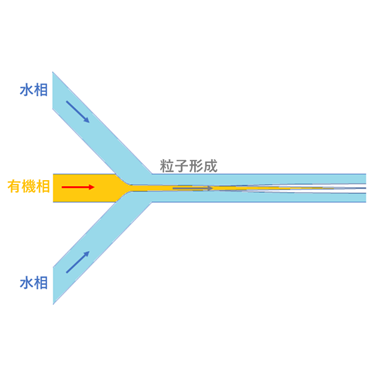
流体力学的流体集束(HFF)構造は、外層液(反溶媒)により内層液(脂質溶液)を集束させ、層流境界面での拡散混合を促進することで、溶媒中に溶解していた脂質を粒子化します。
Staggered Herringbone Mixer(SHM)タイプ

SHMタイプの特徴
-
高い混合効率と再現性
両側から合流する反溶媒の外層液によって脂質溶液を高精度で流路中央部に集束(flow focusing)し、拡散混合させる2D構造を持ちつつ、混合効率を上げるためのヘリンボーン溝も備えています。ジグザグに配置された多数のヘリンボーン溝が層流を細かく分岐・方向転換させ、混合を促進することで脂質の粒子形成を行います。 -
高耐食性
接液部材質はガラス(チップ基板部分)とフッ素樹脂(接続・チューブ配管部分)のみのため、高い耐食性を持ち、様々な溶媒を用いることが可能です。 -
継続使用
作業後に溶媒による洗浄を行うことで、繰り返してご使用いただけます。 -
汎用性
一般的なルアー接続、または1/4-28ネジ接続の接続パーツが予め付加されているため、既存の実験用シリンジポンプ等のマイクロ流体ポンプでもご使用いただけます。特別なノウハウやスキルに依存せず、多様な脂質ナノ粒子(LNP)生成に適用可能です。
送液・装置構成(適合性/対応シリンジポンプ)
※本製品は、弊社製品以外のシリンジポンプを用いて送液することも可能です。
※シリンジポンプをお持ちでない場合は、弊社のマイクロシリンジポンプ MFSPSの導入をご検討ください。
主要な仕様・制御パラメータ(mRNA-LNP/LNP設計のために)
- 30~200nmの粒子径を主に流量制御で制御(総流量、混合流量比)
- μL/min~mL/min単位の流量制御
- 自由なプロトコルと製品構成
製品ラインアップ(LNPSCシリーズ)
LNPSCシリーズの仕様・構成・参考価格については、以下の一覧表をご参照ください。
| 商品コード | 商品名 | チップ材質 | ポート接続 | 標準価格 WEB価格 (税抜) | 在庫目安 通常納期 |
| LNPSC-HFFGH150 | HFFリポソームナノ粒子作製チップ (対応装置ユーザー様用) | ガラス | 5IN/1OUTポート 別途専用コネクター | お問い合わせ | お問い合わせ |
| LNPSC-SHMGHFL | SHMリポソームナノ粒子作製チップキット IN側メスルアー接続 接続チューブ付 | ガラス | 2IN/1OUTポート IN側メスルアー OUTチューブ | ¥166,410 | ~10日程度 (部品在庫時) |
| LNPSC-SHMGHMQ | SHMリポソームナノ粒子作製チップキット IN側オス1/4-28接続 接続チューブ付 | ガラス | 2IN/1OUTポート IN側オス1/4-28 OUTチューブ | ¥166,410 | ~10日程度 (部品在庫時) |
※2026年1月1日現在の情報です。
※急激なコスト変動等により、仕様・価格・構成は予告なく変更される場合があります。
※価格および納期情報はすべて参考値です。
※価格は商流、時期、在庫状況等により変動するため、都度お見積をご依頼ください。
※別途送料(税抜)1,600円/箱(北海道・沖縄は別料金)が発生します。
※LNPSC-HFFGH150チップ本体はドロマイト社製です。
商品カタログ(脂質ナノ粒子・LNP生成)
マイクロ流体シリンジポンプ関連資料
製品使用事例・学術論文(mRNA-LNP研究)
- Hirota M, Tamai M, Yukawa S, et al. Human immune and gut microbial parameters associated with inter-individual variations in COVID-19 mRNA vaccine-induced immunity. Commun Biol. 2023;6(1):368. doi:10.1038/s42003-023-04755-9
- Ogawa K, Tagami T, Miyake S, Ozeki T. Choice of organic solvent affects function of mRNA-LNP; pyridine produces highly functional mRNA-LNP. Int J Pharm. 2025;673:125367. doi:10.1016/j.ijpharm.2025.125367
注意事項
※本シリーズは、試験研究用製品です。
※サンプルのご提供は行っておりませんので、予めご了承ください。

NTサイエンスへのお問い合わせ内容には、通常2営業日以内にご返信致します。
※装置や特注品の御見積は、通常よりもお時間を要する場合がありますので、予めご了承ください。
旧来の050IP電話番号廃止のお知らせ:
事業者のサービス終了に伴い、050-5539で始まる番号は2025年3月31日をもって廃止となりました。
製品お問い合わせや見積依頼は下記お問い合わせフォーム、メール又はFAXにてお願い致します。
ご回答以外の不要な営業アプローチをすることはありませんのでお気軽にお問い合わせください。
◆お問い合わせフォーム
※営業・セールス、スパム、迷惑行為は禁止です。
その他連絡先
◆メール
![]()
※営業・セールス、スパム、迷惑行為は禁止です。
※nt-science.com からのメールをブロック解除し、迷惑メールフォルダをご確認ください。
◆FAX
![]()
※当日受注分:平日17:30まで(土日祝日、休業期間を除く)
参考文献
参考文献を表示(クリックで展開します)
- Björnmalm, Mattias et al. “Engineering and evaluating drug delivery particles in microfluidic devices.” Journal of controlled release vol. 190 (2014): 139-49. doi:10.1016/j.jconrel.2014.04.030
- Carugo, Dario et al. “Liposome production by microfluidics: potential and limiting factors.” Scientific reports vol. 6 25876. 19 May. 2016, doi:10.1038/srep25876
- Cheung, Calvin C L et al. “Microfluidic Production of Lysolipid-Containing Temperature-Sensitive Liposomes.” JoVE ,157 10.3791/60907. 3 Mar. 2020, doi:10.3791/60907
- Cheung, Calvin C L, and Wafa T Al-Jamal. “Sterically stabilized liposomes production using staggered herringbone micromixer: Effect of lipid composition and PEG-lipid content.” International journal of pharmaceutics vol. 566 (2019): 687-696. doi:10.1016/j.ijpharm.2019.06.033
- Hirota M, Tamai M, Yukawa S, et al. Commun Biol. 2023;6(1):368. doi:10.1038/s42003-023-04755-9
- Huang, Xueqin et al. “Microfluidic hydrodynamic focusing synthesis of polymer-lipid nanoparticles for siRNA delivery.” Oncotarget vol. 8,57 96826-96836. 30 May. 2017, doi:10.18632/oncotarget.18281
- Jung, Han Na et al. “Lipid nanoparticles for delivery of RNA therapeutics: Current status and the role of in vivo imaging.” Theranostics vol. 12,17 7509-7531. 24 Oct. 2022, doi:10.7150/thno.77259
- Kastner, Elisabeth et al. “High-throughput manufacturing of size-tuned liposomes…” International journal of pharmaceutics vol. 477 (2014): 361-8. doi:10.1016/j.ijpharm.2014.10.030
- Ogawa K, Tagami T, Miyake S, Ozeki T. Int J Pharm. 2025;673:125367. doi:10.1016/j.ijpharm.2025.125367
- Shepherd, Sarah J et al. “Scalable mRNA and siRNA Lipid Nanoparticle Production…” Nano letters vol. 21,13 (2021): 5671-5680. doi:10.1021/acs.nanolett.1c01353
- Yu, Bo et al. “Microfluidic methods for production of liposomes.” Methods in enzymology vol. 465 (2009): 129-41. doi:10.1016/S0076-6879(09)65007-2
- Zizzari, Alessandra et al. “Continuous-Flow Production of Injectable Liposomes…” Materials vol. 10,12 1411. 10 Dec. 2017, doi:10.3390/ma10121411

